- [04-09]如何检测H7N9禽流感及预防?
- [08-31]LJC-70离子交换纯水器使用说明书
- [07-01]D2010W电动搅拌器使用说明书
- [07-01]H2004G电动搅拌器使用说明书
- [07-01]SH05-3恒温磁力搅拌器使用说明书
- [07-01]H2010G电动搅拌器使用说明书
- [07-01]H2025G电动搅拌器使用说明书
- [07-01]D2025W电动搅拌器使用说明书
- [07-01]D2015W电动搅拌器使用说明书
- [07-01]D2004W电动搅拌器使用说明书
- [12-15]硬度单位换算表,布氏洛氏维氏硬度换算公式
- [02-25]DDS-11A型数字电导率仪说明书
- [03-14]高效液相色谱仪操作步骤
- [07-08]电热蒸馏水器使用说明书
- [06-12]101系列电热鼓风干燥箱使用说明书
- [11-30]电子天平的使用方法
- [12-17]电导率和TDS浓度对照表转换表
- [09-24]游标卡尺如何读数
- [05-04]化学实验中玻璃器皿及实验耗材的使用介绍
- [08-13]在硬度中VpN是什么意思
应用荧光分析技术检测蓝藻生物量的研究2
本课题所采用的三种藻类检测方法中,显微镜计数法采用Olympus BX51光学显微镜在10倍 目镜和10倍物镜下,观察1mm3的血细胞计数板空间中的单细胞藻类数目或者在10μL计数框中的丝状藻类长度。应用荧光分光光度法检测藻蓝蛋白含量和应用可见光分光光度法检测叶绿素a含量分别用到了荧光分光光度计和可见光分光光度计。
3.1 藻蓝蛋白荧光分光光度法的建立
应用荧光分析技术,测定蓝藻中藻蓝蛋白的含量,需要根据荧光激发光谱选择最佳激发光波长,根据荧光发射光谱选择最佳发射波长,在最佳激发波长和最佳发射波长的条件下,测定藻蓝蛋白的荧光强度。在蓝藻中,藻胆蛋白的主要吸收波长为450-660nm的光,藻胆蛋白的吸收光谱是由藻胆素的吸收光谱决定的。藻蓝素的吸收峰位590nm-670nm,藻红素的吸收峰为535nm-567nm,藻尿胆素的吸收峰为498nm,藻胆紫素的吸收峰为598nm[ ]。同时,藻胆蛋白的吸收光谱还与其聚集状态有关,藻胆蛋白的聚集引起吸收峰和吸收系数的红移[ ]。对于蓝藻而言,其藻胆蛋白中以藻蓝蛋白为主,藻蓝蛋白是本课题研究的主要对象。
3.1.1 铜绿微囊藻的荧光光谱簇图
用RF-5301PC型荧光分光光度计扫描铜绿微囊藻的荧光激发光谱簇,如图3-1所示。
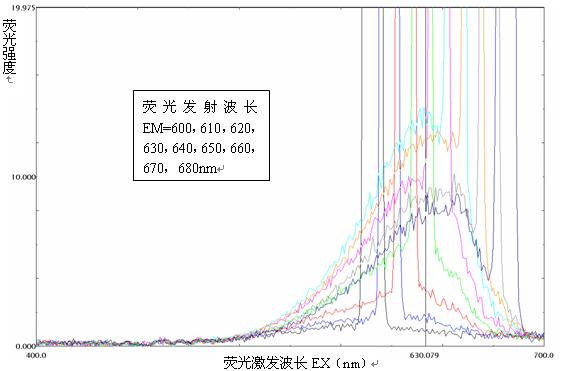
图3-1 铜绿微囊藻的荧光激发光谱簇
观察铜绿微囊藻荧光激发光谱簇中的每一单条曲线,横坐标荧光激发波长在400-700nm的范围内,每条曲线在EX=630nm处均有一峰,因此选用630nm作为最佳激发波长。
观察铜绿微囊藻荧光激发光谱簇中的各条曲线组成的曲线簇,随着荧光发射波长EM由600nm提高到650nm,曲线逐级上升,随着荧光发射波长EM由650nm提高到680nm,曲线逐级下降,当EM=650nm时,曲线为最高位置,峰也为最高峰,因此荧光发射波长为650nm时的荧光强度最强,选用650nm作为最佳发射波长。
用RF-5301PC型荧光分光光度计扫描铜绿微囊藻的荧光发射光谱簇,如图3-2所示。
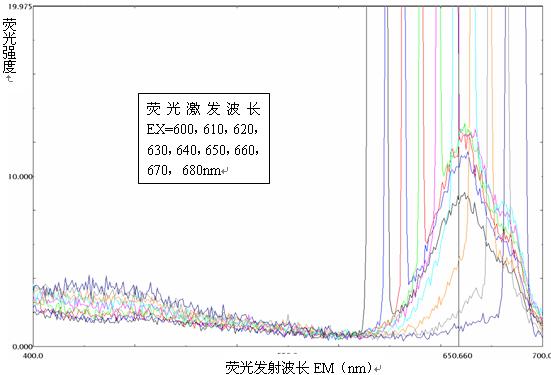
图3-2 铜绿微囊藻的荧光发射光谱簇
观察铜绿微囊藻荧光发射光谱簇中的每一单条曲线,横坐标荧光发射波长在400-700nm的范围内,每条曲线在EM=650nm处均有一峰,因此选用650nm作为最佳发射波长。
观察铜绿微囊藻荧光发射光谱簇中的各条曲线组成的曲线簇,随着荧光激发波长EX由600nm提高到630nm,曲线逐级上升,随着荧光发射波长EX由630nm提高到680nm,曲线逐级下降,当EM=630nm时,曲线为最高位置,峰也为最高峰,因此荧光激发波长为630nm时的荧光强度最强,选用630nm作为最佳激发波长。
3.1.2 钝顶螺旋藻的荧光光谱簇图
用RF-5301PC型荧光分光光度计扫描钝顶螺旋藻的荧光激发光谱簇,如图3-3所示。
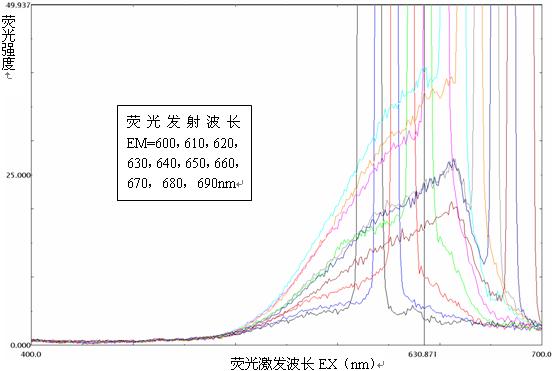
图3-3 钝顶螺旋藻的荧光激发光谱簇
观察钝顶螺旋藻荧光激发光谱簇中的每一单条曲线,横坐标荧光激发波长在400-700nm的范围内,每条曲线在EX=630nm处均有一峰,因此选用630nm作为最佳激发波长。
观察钝顶螺旋藻荧光激发光谱簇中的各条曲线组成的曲线簇,随着荧光发射波长EM由600nm提高到650nm,曲线逐级上升,随着荧光发射波长EM由650nm提高到690nm,曲线逐级下降,当EM=650nm时,曲线为最高位置,峰也为最高峰,因此荧光发射波长为650nm时的荧光强度最强,选用650nm作为最佳发射波长。
用RF-5301PC型荧光分光光度计扫描钝顶螺旋藻的荧光发射光谱簇,如图3-4所示。
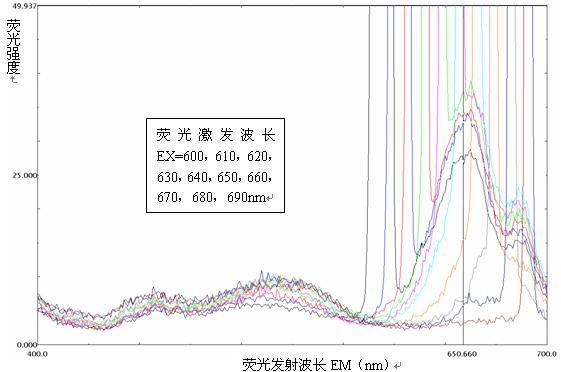
图3-4 钝顶螺旋藻的荧光发射光谱簇
观察钝顶螺旋藻荧光发射光谱簇中的每一单条曲线,横坐标荧光发射波长在400-700nm的范围内,每条曲线在EM=650nm处均有一峰,因此选用650nm作为最佳发射波长。
观察钝顶螺旋藻荧光发射光谱簇中的各条曲线组成的曲线簇,随着荧光激发波长EX由600nm提高到630nm,曲线逐级上升,随着荧光发射波长EX由630nm提高到690nm,曲线逐级下降,当EM=630nm时,曲线为最高位置,峰也为最高峰,因此荧光激发波长为630nm时的荧光强度最强,选用630nm作为最佳激发波长。
3.1.3 斜生栅藻藻的荧光光谱图
用RF-5301PC型荧光分光光度计扫描斜生栅藻的荧光激发光谱,如图3-5所示。

图3-5 斜生栅藻藻的荧光激发光谱
固定EM=650nm,调节EX进行扫描,所得的荧光激发光谱中并没有呈现出明显的峰。
用RF-5301PC型荧光分光光度计扫描斜生栅藻的荧光发射光谱,如图3-6所示。
图3-6 斜生栅藻藻的荧光发射光谱
固定EX=630nm,调节EM进行扫描,所得的荧光发射光谱中在650nm处并没有呈现出明显的峰,而在680nm处出现明显的峰,但此处的峰是叶绿素a的荧光特征峰,并不是藻蓝蛋白的荧光特征峰[ ]。
由斜生栅藻的荧光激发光谱和荧光发射光谱,可以看出绿藻中不含有藻蓝蛋白。
综上所述,选用荧光激发波长EX=630nm,荧光发射波长EM=650nm作为荧光分光光度法检测藻蓝蛋白含量的最佳波长值。
3.2 叶绿素a可见光分光光度法的建立
叶绿素a在红光区和蓝光区各有一个吸收峰,在绿光区(450-650nm之间)仅有很弱的吸收,因此呈现绿色。研究表明叶绿素a是与蛋白结合在一起,起捕获光能作用的是色素和蛋白形成的复合体,称之为捕光色素蛋白复合体,它属于光系统的天线系统。叶绿素a与蛋白相互作用的一个重要结果是色素的吸收光谱发生改变,叶绿素a在有机溶剂中的吸收峰(661-667nm之间)位于红光区,在活细胞或叶绿体中的叶绿素a的吸收峰的位置比在有机溶剂中的吸收峰红移了10-15nm,大致在红光区(680nm左右)[ ]。
3.2.1 铜绿微囊藻的可见光吸收光谱图
用UV-2102 PCS型紫外可见分光光度计扫描铜绿微囊藻的可见光吸收光谱,如图3-7所示。
图3-7 铜绿微囊藻的可见光吸收光谱
观察铜绿微囊藻吸收光谱,在400-700nm的可见光区域内,其一最大吸收峰大约在682nm处,此峰为叶绿素a在活细胞或叶绿体中的吸收峰,因此选用682nm处的吸光度检测铜绿微囊藻中的叶绿素a含量。
3.2.2 钝顶螺旋藻的可见光吸收光谱图
用UV-2102 PCS型紫外可见分光光度计扫描钝顶螺旋藻的可见光吸收光谱,如图3-8所示。
图3-8 钝顶螺旋藻的可见光吸收光谱
观察钝顶螺旋藻吸收光谱,在400-700nm的可见光区域内,其一最大吸收峰大约在682nm处,此峰为叶绿素a在活细胞或叶绿体中的吸收峰,因此选用682nm出的吸光度检测钝顶螺旋藻中的叶绿素a含量。
3.2.3 斜生栅藻的可见光吸收光谱图
用UV-2102 PCS型紫外可见分光光度计扫描斜生栅藻的可见光吸收光谱,如图3-9所示。
图3-9 斜生栅藻的可见光吸收光谱
观察斜生栅藻藻吸收光谱,在400-700nm的可见光区域内,其一最大吸收峰大约在682nm处,此峰为叶绿素a在活细胞或叶绿体中的吸收峰,因此选用682nm出的吸光度检测斜生栅藻中的叶绿素a含量。
综上所述,选用682nm作为可见光分光光度法检测叶绿素a含量的最佳波长值。
第4章 荧光检测关系的建立
由上一章内容,研究得到三种藻类检测方法的具体操作方式。本章将通过这三种方法建立藻类荧光检测的工作曲线。
4.1 实验设计
接种培养两种蓝藻(铜绿微囊藻和钝顶螺旋藻)和一种绿藻(斜生栅藻)至生长稳定期,分别在各浓度下测量三个生物指标(藻细胞浓度或藻细胞长度、藻蓝蛋白荧光强度、叶绿素a可见光吸光度),建立藻蓝蛋白荧光强度、叶绿素a可见光吸光度分别对藻细胞浓度或
藻细胞长度的工作曲线。其中,藻细胞浓度采用血细胞计数板法测量,藻细胞长度采用10μL计数框法测量,藻蓝蛋白荧光强度采用EX=630nm,EM=650nm荧光分光光度法测量,叶绿素a可见光吸光度采用682nm可见光分光光度法测量。
4.2 实验结果
4.2.1 铜绿微囊藻工作曲线
表4-1 铜绿微囊藻生物指标数值表
|
生物指标 |
数值 | |||||
|
藻细胞浓度C(×105cell/mL) |
1.75 |
8.75 |
17.50 |
35.00 |
87.50 |
175.00 |
|
藻蓝蛋白荧光强度I630-650 |
1.750 |
6.214 |
13.970 |
26.520 |
55.848 |
95.590 |
|
叶绿素a可见光吸光度A682 |
0.009 |
0.041 |
0.081 |
0.160 |
0.403 |
0.736 |
图4-1 铜绿微囊藻工作曲线
藻细胞浓度在105cell/mL-107cell/mL的范围内,线性拟合铜绿微囊藻藻蓝蛋白荧光强度工作曲线I630-650=0.5727C,C为藻细胞浓度,单位×105cell/mL。相关系数R2=0.9826。
藻细胞浓度在105cell/mL-107cell/mL的范围内,线性拟合铜绿微囊藻叶绿素a可见光吸光度工作曲线A682=0.0043C,C为藻细胞浓度,单位×105cell/mL。相关系数R2=0.9972。
4.2.2 钝顶螺旋藻工作曲线
表4-2 钝顶螺旋藻生物指标数值表
|
生物指标 |
数值 | ||||
|
藻细胞长度L(×102mm/mL) |
2.73 |
13.65 |
68.25 |
136.50 |
341.25 |
|
藻蓝蛋白荧光强度I630-650 |
0.651 |
3.302 |
13.951 |
24.045 |
45.830 |
|
叶绿素a可见光吸光度A682 |
0.005 |
0.042 |
0.185 |
0.373 |
0.746 |
图4-2 钝顶螺旋藻工作曲线
藻细胞长度在102mm/mL-105mm/mL的范围内,线性拟合钝顶螺旋藻藻蓝蛋白荧光强度工作曲线I630-650=0.1424L,L为藻细胞长度,单位×102mm/mL。相关系数R2=0.9638。
藻细胞长度在102mm/mL-105mm/mL的范围内,线性拟合钝顶螺旋藻叶绿素a可见光吸光度工作曲线A682=0.0023L,L为藻细胞长度,单位×102mm/mL。相关系数R2=0.9970。
4.2.3斜生栅藻工作曲线
表4-3 斜生栅藻生物指标数值表
|
生物指标 |
数值 | |||||
|
藻细胞浓度C(×105cell/mL) |
1.00 |
5.00 |
10.00 |
20.00 |
50.00 |
100.00 |
|
藻蓝蛋白荧光强度I630-650 |
0.343 |
0.482 |
0.630 |
0.913 |
1.610 |
2.590 |
|
叶绿素a可见光吸光度A682 |
0.006 |
0.025 |
0.054 |
0.103 |
0.274 |
0.499 |
图4-3 斜生栅藻工作曲线
藻细胞浓度在105cell/mL-107cell/mL的范围内,线性拟合斜生栅藻藻蓝蛋白荧光强度工作曲线I630-650=0.0282C,C为藻细胞浓度,单位×105cell/mL。相关系数R2=0.8507。
藻细胞浓度在105cell/mL-107cell/mL的范围内,线性拟合斜生栅藻叶绿素a可见光吸光度工作曲线A682=0.0051C,C为藻细胞浓度,单位×105cell/mL。相关系数R2=0.9973。
4.3 实验讨论
通过两种蓝藻(铜绿微囊藻和钝顶螺旋藻)的工作曲线,可以看出随着藻细胞浓度或者藻细胞长度的增大,藻液中的藻蓝蛋白荧光强度和叶绿素a可见光吸光度随之增大,呈现出良好的线性关系。由此说明,随着蓝藻生物量的增长,藻液中的特征色素体藻蓝蛋白的含量随之增长,藻液中的叶绿素a的含量也随之增长。
通过一种绿藻(斜生栅藻)的工作曲线,可以看出随着藻细胞浓度的增大,藻液中叶绿素a可见光吸光度随之增大,呈现出良好的线性关系。但是藻液中的藻蓝蛋白荧光强度值一直保持在很低的水平,与两种蓝藻藻液中的藻蓝蛋白荧光强度相比,其值十分微小。由此说明,随着绿藻生物量的增长,藻液中的叶绿素a含量随之增长,但是由于绿藻中不含有藻蓝蛋白,所以藻液中的藻蓝蛋白荧光强度十分微小,可以忽略不计。这是利用特征色素体区分蓝藻和绿藻的突破点,也证明了应用荧光分析技术选择性的检测蓝藻生物量的可行性。
第5章 不同生长条件的荧光检测关系的研究
本章在前一章的基础上研究两种蓝藻(铜绿微囊藻和钝顶螺旋藻)在不同光照强度下的藻蓝蛋白荧光强度工作曲线簇,并对工作曲线簇进行讨论,研究不同光照强度下有着不同生长速率的蓝藻的光学特性变化。
5.1 实验设计
接种两种蓝藻(铜绿微囊藻和钝顶螺旋藻),于6个不同光照强度(800lx、1600lx、3200lx、5400lx、8000lx和12000lx)下培养两种蓝藻至其生长稳定期,分别稀释至各浓度或长度,测定其藻细胞浓度或藻细胞长度、藻蓝蛋白荧光强度、叶绿素a可见光吸光度三个
生物指标,作出不同光照强度下两种蓝藻的藻蓝蛋白荧光强度工作曲线簇和叶绿素a可见光吸光度工作曲线簇,研究在不同光强下有着不同生长速率的蓝藻的光学特性的变化。其中,藻细胞浓度采用血细胞计数板法测量,藻细胞长度采用10μL计数框法测量,藻蓝蛋白荧光强度采用EX=630nm,EM=650nm荧光分光光度法测量,叶绿素a可见光吸光度采用682nm可见光分光光度法测量。
5.2 实验结果
5.2.1 铜绿微囊藻不同光强下的工作曲线簇
铜绿微囊藻不同光强下的各项生物指标见表5-1。
表5-1 铜绿微囊藻不同光强下生物指标数值表
|
光照强度 |
生物指标 |
数值 | |||||
|
800lx |
藻细胞浓度C(×105cell/mL) |
1.50 |
7.50 |
15.00 |
30.00 |
75.00 |
150.00 |
|
|
藻蓝蛋白荧光强度I630-650 |
2.123 |
6.345 |
12.762 |
24.550 |
54.010 |
92.560 |
|
|
叶绿素a可见光吸光度A682 |
0.007 |
0.036 |
0.077 |
0.152 |
0.377 |
0.720 |
|
1600lx |
藻细胞浓度C(×105cell/mL) |
1.75 |
8.75 |
17.50 |
35.00 |
87.50 |
175.00 |
|
|
藻蓝蛋白荧光强度I630-650 |
1.750 |
6.214 |
13.970 |
26.520 |
55.848 |
95.590 |
|
|
叶绿素a可见光吸光度A682 |
0.009 |
0.041 |
0.081 |
0.160 |
0.403 |
0.736 |
|
3200lx |
藻细胞浓度C(×105cell/mL) |
1.430 |
7.150 |
14.300 |
28.600 |
71.500 |
143.00 |
|
|
藻蓝蛋白荧光强度I630-650 |
0.876 |
2.592 |
4.288 |
8.061 |
18.105 |
33.447 |
|
|
叶绿素a可见光吸光度A682 |
0.006 |
0.024 |
0.058 |
0.102 |
0.224 |
0.415 |
|
5600lx |
藻细胞浓度C(×105cell/mL) |
1.63 |
8.15 |
16.30 |
32.60 |
81.50 |
163.00 |
|
|
藻蓝蛋白荧光强度I630-650 |
0.313 |
1.735 |
3.413 |
8.580 |
17.333 |
34.568 |
|
|
叶绿素a可见光吸光度A682 |
0.005 |
0.019 |
0.040 |
0.086 |
0.213 |
0.431 |
|
8000lx |
藻细胞浓度C(×105cell/mL) |
1.70 |
8.50 |
17.00 |
34.00 |
85.00 |
170.00 |
|
|
藻蓝蛋白荧光强度I630-650 |
0.288 |
1.011 |
1.542 |
3.987 |
10.310 |
22.483 |
|
|
叶绿素a可见光吸光度A682 |
0.003 |
0.012 |
0.024 |
0.055 |
0.120 |
0.251 |
|
12000lx |
藻细胞浓度C(×105cell/mL) |
1.81 |
9.05 |
18.10 |
36.20 |
90.50 |
181.00 |
|
|
藻蓝蛋白荧光强度I630-650 |
0.531 |
0.665 |
1.347 |
3.114 |
8.258 |
20.369 |
|
|
叶绿素a可见光吸光度A682 |
0.002 |
0.008 |
0.020 |
0.050 |
0.120 |
0.256 |
铜绿微囊藻不同光强下的藻蓝蛋白荧光强度工作曲线簇如图5-1。
图5-1铜绿微囊藻不同光强下藻蓝蛋白荧光强度工作曲线簇铜绿微囊藻藻细胞浓度在105cell/mL-107cell/mL的范围内,线性拟合各光照强度下铜绿微囊藻藻蓝蛋白荧光强度工作曲线,见表5-2。
表5-2 铜绿微囊藻不同光强下藻蓝蛋白荧光强度工作曲线簇线性拟合结果表
|
光照强度 |
线性拟合工作曲线 |
斜率 |
相关系数 |
|
800lx |
I630-650 = 0.6453C |
0.6453 (×105cell/mL)-1 |
0.9854 |
|
1600lx |
I630-650 = 0.5727C |
0.5727 (×105cell/mL)-1 |
0.9826 |
|
3200lx |
I630-650 = 0.2399C |
0.2399 (×105cell/mL)-1 |
0.9938 |
|
5600lx |
I630-650 = 0.2317C |
0.2317 (×105cell/mL)-1 |
0.9969 |
|
8000lx |
I630-650 = 0.1293C |
0.1293 (×105cell/mL)-1 |
0.9964 |
|
12000lx |
I630-650 = 0.1073C |
0.1073 (×105cell/mL)-1 |
0.9861 |
铜绿微囊藻不同光强下的叶绿素a可见光吸光度工作曲线簇如图5-2。
图5-2 铜绿微囊藻不同光强下叶绿素a可见光吸光度工作曲线簇
铜绿微囊藻藻细胞浓度在105cell/mL-107cell/mL的范围内,线性拟合各光照强度下铜绿微囊藻叶绿素a可见光吸光度工作曲线,见表5-3。
表5-3 铜绿微囊藻不同光强下叶绿素a可见光吸光度工作曲线簇线性拟合结果表
|
光照强度 |
线性拟合工作曲线 |
斜率 |
相关系数 |
|
800lx |
A682 = 0.0049C |
0.0049(×105cell/mL)-1 |
0.9992 |
|
1600lx |
A682 = 0.0043C |
0.0043(×105cell/mL)-1 |
0.9972 |
|
3200lx |
A682 = 0.0030C |
0.0030(×105cell/mL)-1 |
0.9937 |
|
5600lx |
A682 = 0.0026C |
0.0026 (×105cell/mL)-1 |
0.9998 |
|
8000lx |
A682 = 0.0015C |
0.0015 (×105cell/mL)-1 |
0.9988 |
|
12000lx |
A682 = 0.0014C |
0.0014(×105cell/mL)-1 |
0.9979 |
5.2.2 钝顶螺旋藻在不同光强下的工作曲线簇钝顶螺旋藻不同光强下的各项生物指标见表5-4。
表5-4 钝顶螺旋藻不同光强下生物指标数值表
|
光照强度 |
生物指标 |
数值 | |||||
|
800lx |
藻细胞长度L(×102mm/mL)) |
2.52 |
12.60 |
63.00 |
126.00 |
315.00 |
630.00 |
|
|
藻蓝蛋白荧光强度I630-650 |
1.123 |
3.345 |
13.762 |
24.550 |
54.010 |
92.560 |
|
|
叶绿素a可见光吸光度A682 |
0.007 |
0.036 |
0.165 |
0.391 |
0.886 |
1.781 |
|
1600lx |
藻细胞长度L(×102mm/mL)) |
2.73 |
13.65 |
68.25 |
136.50 |
341.25 |
682.50 |
|
|
藻蓝蛋白荧光强度I630-650 |
0.651 |
3.302 |
13.951 |
24.045 |
45.830 |
88.061 |
|
|
叶绿素a可见光吸光度A682 |
0.005 |
0.042 |
0.185 |
0.373 |
0.746 |
1.646 |
|
3200lx |
藻细胞长度L(×102mm/mL)) |
2.85 |
14.25 |
71.25 |
142.50 |
356.25 |
712.50 |
|
|
藻蓝蛋白荧光强度I630-650 |
0.225 |
2.592 |
11.784 |
22.248 |
42.378 |
80.012 |
|
|
叶绿素a可见光吸光度A682 |
0.004 |
0.030 |
0.155 |
0.271 |
0.711 |
1.429 |
|
5600lx |
藻细胞长度L(×102mm/mL)) |
3.02 |
15.10 |
75.50 |
151.00 |
377.50 |
755.00 |
|
|
藻蓝蛋白荧光强度I630-650 |
0.200 |
1.884 |
7.877 |
14.980 |
32.157 |
70.123 |
|
|
叶绿素a可见光吸光度A682 |
0.003 |
0.022 |
0.108 |
0.214 |
0.505 |
1.125 |
|
8000lx |
藻细胞长度L(×102mm/mL)) |
3.12 |
15.60 |
78.00 |
156.00 |
390.00 |
780.00 |
|
|
藻蓝蛋白荧光强度I630-650 |
0.124 |
0.999 |
4.886 |
10.965 |
25.140 |
57.128 |
|
|
叶绿素a可见光吸光度A682 |
0.003 |
0.021 |
0.090 |
0.166 |
0.477 |
0.950 |
|
12000lx |
藻细胞长度L(×102mm/mL)) |
3.26 |
16.30 |
81.50 |
163.00 |
407.50 |
815.00 |
|
|
藻蓝蛋白荧光强度I630-650 |
0.081 |
0.512 |
2.898 |
6.782 |
18.253 |
38.544 |
|
|
叶绿素a可见光吸光度A682 |
0.001 |
0.011 |
0.046 |
0.100 |
0.280 |
0.580 |
钝顶螺旋藻不同光强下的藻蓝蛋白荧光强度工作曲线簇如图5-3。
图5-3 钝顶螺旋藻不同光强下藻蓝蛋白荧光强度工作曲线簇钝顶螺旋藻藻细胞长度在102mm/mL-105mm/mL的范围内,线性拟合各光照强度下钝顶螺旋藻藻蓝蛋白荧光强度工作曲线,见表5-5。
表5-5 钝顶螺旋藻不同光强下藻蓝蛋白荧光强度工作曲线簇线性拟合结果表
|
光照强度 |
线性拟合工作曲线 |
斜率 |
相关系数 |
|
800lx |
I630-650 = 0.1537C |
0.1537 (×102mm/mL)-1 |
0.9849 |
|
1600lx |
I630-650 = 0.1321C |
0.1321 (×102mm/mL)-1 |
0.9876 |
|
3200lx |
I630-650 = 0.1154C |
0.1154 (×102mm/mL)-1 |
0.9883 |
|
5600lx |
I630-650 = 0.0917C |
0.0917 (×102mm/mL)-1 |
0.9974 |
|
8000lx |
I630-650 = 0.0714C |
0.0714 (×102mm/mL)-1 |
0.9959 |
|
12000lx |
I630-650 = 0.0465C |
0.0465 (×102mm/mL)-1 |
0.9979 |
钝顶螺旋藻不同光强下的叶绿素a可见光吸光度工作曲线簇如图5-4。
图5-4 钝顶螺旋藻不同光强下叶绿素a可见光吸光度工作曲线簇
钝顶螺旋藻藻细胞长度在102mm/mL-105mm/mL的范围内,线性拟合各光照强度下钝顶螺旋藻叶绿素a可见光吸光度工作曲线,见表5-6。
表5-6 钝顶螺旋藻不同光强下叶绿素a可见光吸光度工作曲线簇线性拟合结果表
|
光照强度 |
线性拟合工作曲线 |
斜率 |
相关系数 |
|
800lx |
A682 = 0.0028C |
0.0028 (×102mm/mL)-1 |
0.9974 |
|
1600lx |
A682 = 0.0023C |
0.0023 (×102mm/mL)-1 |
0.9841 |
|
3200lx |
A682 = 0.0020C |
0.0020 (×102mm/mL)-1 |
0.9990 |
|
5600lx |
A682 = 0.0014C |
0.0014 (×102mm/mL)-1 |
0.9990 |
|
8000lx |
A682 = 0.0012C |
0.0012 (×102mm/mL)-1 |
0.9963 |
|
12000lx |
A682 = 0.0007C |
0.0007 (×102mm/mL)-1 |
0.9960 |
5.3 实验讨论
在不同的光照强度下,蓝藻具有不同的生长速率,藻细胞表现出的光学特性也不同。宏观角度观察,随着光照强度的逐渐增大,蓝藻在培养的过程中颜色逐渐由蓝绿向淡绿向黄绿转变,藻液颜色逐渐变淡。微观角度观察,随着光照强度的逐渐增大,蓝藻的工作曲线的逐级下降,曲线斜率逐渐减小,表明单位藻细胞中的藻蓝蛋白含量逐渐减少,叶绿素a含量也逐渐减少。
分析其原因,蓝藻中的三类光合色素——叶绿素、类胡萝卜素和藻胆素的功能作用各不相同,光照条件的改变会引起细胞内色素比例的改变[ , ],光强增大,会导致叶绿素和其他光合色素含量的降低[ ]。
藻蓝蛋白作为蓝藻的特征色素体,在藻细胞中以较大的聚集物——藻胆体的形式存在,藻胆体是一群结合在类囊体外表面的直径为32-70nm、高度为25-45nm、厚度为12-40nm的颗粒,一般呈半圆盘状、半椭球状、捆状或块状,其结构由中央的“核”(Core)和外周的“棒”(Rod)两部分组成。藻胆体在类囊体表面的分布不是随机的,而是有一定的秩序,并且每一个藻胆体中均含有几种不同的藻胆蛋白。藻胆体作为蓝藻的捕光体,起捕获光能并传递到反应中心的作用。当光照强度增大时,单位藻胆体捕获的光能增大,所以在保证光能总需求量不变的情况下,藻胆体的数目可以减少,导致藻蓝蛋白含量降低。Grossmanet等人在1994年的研究中也发现低光照强度可能会刺激合成藻蓝蛋白,高光照强度可能会抑
制合成藻蓝蛋白[ ]。
叶绿素a一方面作为捕光色素,和蛋白结合成叶绿素a蛋白复合体,捕获光能供给光合作用,另一方面还是蓝藻光合作用的反应中心色素。单位藻细胞中叶绿素a的含量随着光照水平增加而递减的趋势,反映了藻类对于光能利用具有较强的主动性,即藻类能够通过调节自身的光合色素的含量来控制对光能的利用能力[ ]。
第6章 不同生长阶段的荧光检测关系的研究
本章在前两章的基础上研究两种蓝藻(铜绿微囊藻和钝顶螺旋藻)在各自的生长周期中处于不同生长阶段时,藻细胞中藻蓝蛋白的荧光强度工作曲线簇。并对两个工作曲线簇进行讨论,研究不同生长阶段中有着不同生长速率的蓝藻的光学特性变化。
6.1 实验设计
接种两种蓝藻(铜绿微囊藻和钝顶螺旋藻),于1600lx光照强度下培养一个完整的生命周期,每隔一天测定藻液中藻细胞个数或者长度,作出蓝藻一个生命周期的生长曲线。选取迟缓期、生长期和稳定期三个特征时期的藻液,分别稀释至各浓度或长度,测定其藻细胞浓度或藻细胞长度、藻蓝蛋白荧光强度、叶绿素a可见光吸光度三个生物指标,作出不同生长阶段中两种蓝藻的藻蓝蛋白荧光强度工作曲线簇和叶绿素a可见光吸光度工作曲线簇,研究在不同生长阶段中有着不同生长速率的蓝藻的光学特性的变化。其中,藻细胞浓度采用血细胞计数板法测量,藻细胞长度采用10μL计数框法测量,藻蓝蛋白荧光强度采用EX=630nm,EM=650nm荧光分光光度法测量,叶绿素a可见光吸光度采用682nm可见光分光光度法测量。
6.2 实验结果
6.2.1 铜绿微囊藻生长曲线
实验期间,摇瓶藻液随着培养时间的水色变化情况如图6-1所示。接种后前5天水色变化不大,第7天开始泛绿,第10天变成浅绿色,第15天已成翠绿,第23天水色继续加深,摇瓶底部出现少量死亡藻细胞,第33天水色变成墨绿色,并伴有部分死亡藻细胞沉淀。第40天藻液依然处于稳定生长期,水色基本趋于墨绿色不变化。
图6-1 铜绿微囊藻藻液随培养时间的变化
实验期间铜绿微囊藻生长曲线如图6-2所示,接种时的藻细胞浓度为5×105cell/mL,培养40天后。藻细胞浓度为1×108cell/mL。
图6-2 铜绿微囊藻生长曲线
6.2.2 铜绿微囊藻在不同生长阶段中的工作曲线簇
观察铜绿微囊藻生长曲线图,选取第5天、第19天和第33天的藻液分别作为迟缓期、生长期和稳定期的研究对象进行三个生物指标的测定。数据如表6-1所示。
表6-1 铜绿微囊藻不同生长阶段中生物指标数值表
|
生长阶段 |
生物指标 |
数值 | |||||
|
迟缓期 |
藻细胞浓度C(×105cell/mL) |
0.13 |
0.26 |
0.52 |
1.30 |
2.60 |
13.00 |
|
|
藻蓝蛋白荧光强度I630-650 |
0.065 |
0.112 |
0.271 |
0.823 |
1.464 |
6.409 |
|
|
叶绿素a可见光吸光度A682 |
0.001 |
0.001 |
0.002 |
0.004 |
0.011 |
0.050 |
|
生长期 |
藻细胞浓度C(×105cell/mL) |
1.16 |
5.80 |
11.60 |
23.20 |
58.00 |
116.00 |
|
|
藻蓝蛋白荧光强度I630-650 |
0.887 |
4.681 |
8.369 |
12.936 |
31.325 |
67.333 |
|
|
叶绿素a可见光吸光度A682 |
0.005 |
0.031 |
0.068 |
0.121 |
0.298 |
0.504 |
|
稳定期 |
藻细胞浓度C(×105cell/mL) |
1.02 |
2.04 |
10.20 |
20.40 |
40.80 |
102.00 |
|
|
藻蓝蛋白荧光强度I630-650 |
0.584 |
3.007 |
4.523 |
10.508 |
20.146 |
54.324 |
|
|
叶绿素a可见光吸光度A682 |
0.004 |
0.007 |
0.046 |
0.089 |
0.193 |
0.415 |
铜绿微囊藻不同生长阶段中的藻蓝蛋白荧光强度工作曲线簇如图6-3。
图6-3 铜绿微囊藻不同生长阶段中藻蓝蛋白荧光强度工作曲线簇铜绿微囊藻藻细胞浓度在105cell/mL-107cell/mL的范围内,线性拟合各生长阶段中铜绿微囊藻藻蓝蛋白荧光强度工作曲线,见表6-2。
表6-2 铜绿微囊藻不同生长阶段中藻蓝蛋白荧光强度工作曲线簇线性拟合结果表
|
生长阶段 |
线性拟合工作曲线 |
斜率 |
相关系数 |
|
迟缓期 |
I630-650= 0.4970C |
0.4970 (×105cell/mL)-1 |
0.9979 |
|
生长期 |
I630-650= 0.5735C |
0.5735 (×105cell/mL)-1 |
0.9970 |
|
稳定期 |
I630-650= 0.5265C |
0.5265 (×105cell/mL)-1 |
0.9967 |
铜绿微囊藻不同生长阶段中的叶绿素a可见光吸光度工作曲线簇如图6-4。
图6-4 铜绿微囊藻不同生长阶段中叶绿素a可见光吸光度工作曲线簇
铜绿微囊藻藻细胞浓度在105cell/mL-107cell/mL的范围内,线性拟合各生长阶段中铜绿微囊藻叶绿素a可见光吸光度工作曲线,见表6-3。
表6-3 铜绿微囊藻不同生长阶段中叶绿素a可见光吸光度工作曲线簇线性拟合结果表
|
生长阶段 |
线性拟合工作曲线 |
斜率 |
相关系数 |
|
迟缓期 |
A682 = 0.0039C |
0.0039 (×105cell/mL)-1 |
0.9988 |
|
生长期 |
A682 = 0.0045C |
0.0045 (×105cell/mL)-1 |
0.9882 |
|
稳定期 |
A682 = 0.0042C |
0.0042 (×105cell/mL)-1 |
0.9947 |
6.2.3 钝顶螺旋藻生长曲线
实验期间钝顶螺旋藻生长曲线如图6-5所示,接种时的藻细胞长度为5×102mm/mL,培养40天后。藻细胞长度为1×105mm/mL。
图6-5 钝顶螺旋藻生长曲线
6.2.4 钝顶螺旋藻在不同生长阶段中的工作曲线簇观察钝顶螺旋藻生长曲线图,选取第7天、第19天和第35天的藻液分别作为迟缓期、生长期和稳定期的研究对象进行三个生物指标的测定。数据如表6-4所示。
表6-4 钝顶螺旋藻不同生长阶段中生物指标数值表
|
生长阶段 |
生物指标 |
数值 |
| ||||
|
迟缓期 |
藻细胞长度L(×102mm/mL) |
0.15 |
0.74 |
3.70 |
7.40 |
18.50 |
37.00 |
|
|
藻蓝蛋白荧光强度I630-650 |
0.002 |
0.005 |
0.333 |
0.612 |
1.758 |
3.624 |
|
|
叶绿素a可见光吸光度A682 |
0.001 |
0.002 |
0.008 |
0.016 |
0.042 |
0.075 |
|
生长期 |
藻细胞长度L(×102mm/mL) |
2.00 |
10.00 |
50.00 |
100.00 |
250.00 |
500.00 |
|
|
藻蓝蛋白荧光强度I630-650 |
0.210 |
1.222 |
5.368 |
11.852 |
36.241 |
65.054 |
|
|
叶绿素a可见光吸光度A682 |
0.006 |
0.041 |
0.125 |
0.245 |
0.687 |
1.228 |
|
稳定期 |
藻细胞长度L(×102mm/mL) |
3.61 |
18.06 |
90.30 |
180.60 |
451.50 |
903.00 |
|
|
藻蓝蛋白荧光强度I630-650 |
0.315 |
1.655 |
9.980 |
23.360 |
54.210 |
98.365 |
|
|
叶绿素a可见光吸光度A682 |
0.006 |
0.040 |
0.188 |
0.420 |
1.000 |
1.980 |
钝顶螺旋藻藻不同生长阶段中的藻蓝蛋白荧光强度工作曲线簇如图6-6。
图6-6 钝顶螺旋藻不同生长阶段中藻蓝蛋白荧光强度工作曲线簇
钝顶螺旋藻藻细胞长度在102mm/mL-105mm/mL的范围内,线性拟合各生长阶段中钝顶螺旋藻藻蓝蛋白荧光强度工作曲线,见表6-5。
表6-5 钝顶螺旋藻不同生长阶段中藻蓝蛋白荧光强度工作曲线簇线性拟合结果表
|
生长阶段 |
线性拟合工作曲线 |
斜率 |
相关系数 |
|
迟缓期 |
I630-650= 0.0968C |
0.0968 ((×102mm/mL)-1 |
0.9981 |
|
生长期 |
I630-650= 0.1324C |
0.1324 ((×102mm/mL)-1 |
0.9956 |
|
稳定期 |
I630-650= 0.1117C |
0.1117 ((×102mm/mL)-1 |
0.9958 |
钝顶螺旋藻不同生长阶段中的叶绿素a可见光吸光度工作曲线簇如图6-7。
图6-7 钝顶螺旋藻不同生长阶段中叶绿素a可见光吸光度工作曲线簇
钝顶螺旋藻藻细胞长度在102mm/mL-105mm/mL的范围内,线性拟合各生长阶段中钝顶螺旋藻叶绿素a可见光吸光度工作曲线,见表6-6。
表6-6 钝顶螺旋藻不同生长阶段中叶绿素a可见光吸光度工作曲线簇线性拟合结果表
|
生长阶段 |
线性拟合工作曲线 |
斜率 |
相关系数 |
|
迟缓期 |
A682 = 0.0021C |
0.0021 ((×102mm/mL)-1 |
0.9959 |
|
生长期 |
A682 = 0.0027C |
0.0027 ((×102mm/mL)-1 |
0.9965 |
|
稳定期 |
A682 = 0.0022C |
0.0022 ((×102mm/mL)-1 |
0.9992 |
6.3 实验讨论
6.3.1 关于两种蓝藻的生长曲线
蓝藻细胞在低浓度接种到新培养基中,藻细胞内各种酶系统对新环境存在一个适应过程,藻细胞浓度上升较缓慢,存在短暂的环境适应期,这个阶段称之为迟缓期;迟缓期过后,藻细胞数量迅猛增长,此时,因为藻内酶系统对新环境已基本适应,藻细胞个体发育也达到了一定的程度,细胞增殖比较快,尤其是后期藻细胞数量增长迅速,生长曲线呈对数上升,这个阶段称之为生长期,此时藻细胞大量繁衍、增殖,营养物质也被大量消耗,可能成为藻细胞增殖的限制因素;生长期过后,藻细胞增殖在一定程度上受到营养盐的限制,虽然稳定生长,但增殖速度较慢,几乎和细胞衰亡速率相等,生物量达到最高水平,这一阶段称为稳定期;稳定期过后,藻细胞数量会有下降的趋势,随着营养物质含量持续下降并达到近乎耗尽的程度,藻细胞开始利用自身内储存的物质,进行内源代谢,大量细胞衰亡,这个阶段称之为衰亡期。本实验中,所培养两种蓝藻均经历了迟缓期、生长期和稳定期,但是由于稳定期持续时间较长,并没有在所观察的时间内监测到蓝藻进入衰亡期的迹
象。
6.3.2 关于两种蓝藻不同生长阶段的工作曲线簇
以铜绿微囊藻不同生长阶段的藻蓝蛋白荧光强度的工作曲线簇为例,从迟缓期到生长期再到稳定期,工作曲线先抬升后下降,工作曲线的斜率先增大后减小,这表明单个藻细胞内的藻蓝蛋白含量从迟缓期到生长期逐渐上升,从生长期到稳定期逐渐下降。分析其原因,第一阶段迟缓期中藻细胞处于适应状态,细胞内各种酶系统对新环境存在一个适应过程,细胞内的光合色素开始合成,但含量较低,所以单个细胞内的天线色素体藻蓝蛋白含量较低;第二阶段生长期中藻细胞内酶系统对新环境已基本适应,藻细胞个体发育也达到了一定的程度,细胞内的光合色素大量合成,含量增大,同时由于藻细胞有分裂生殖的需要,必须大量获取光能,光合色素的含量达到了最高,所以单个藻细胞内的藻蓝蛋白含量高;第三阶段稳定期中藻细胞的增殖速率等于衰亡速率,藻液中有大量成熟的藻细胞,也开始有衰亡的藻细胞,所以虽然藻液中藻细胞浓度达到最高点,但是除以总藻细胞个数平均下来,每个藻细胞中的光合素色含量没有生长期高,但比迟缓期要高,所以单个藻细胞内的藻蓝蛋白含量介于迟缓期和生长期之间;第四个阶段衰亡期,虽然没有建立铜绿微囊藻衰亡期的藻蓝蛋白荧光强度的工作曲线,但是可以推测,衰亡期细胞进入程序死亡阶段,细胞开始利用自身内储存的物质进行内源代谢,细胞内的光合色素含量降低,单个藻细胞内
的藻蓝蛋白含量降低。
同样,铜绿微囊藻不同生长阶段的叶绿素a含量可见光吸光度、钝顶螺旋藻不同生长阶段的藻蓝蛋白荧光强度、钝顶螺旋藻不同生长阶段的叶绿素a含量可见光吸光度等三个工作曲线簇也可以用同样的蓝藻生长周期理论进行解释分析[ ]。
第7章 结论和展望
7.1结论
本课题分为四个阶段。第一阶段建立蓝藻的荧光检测方法。完成了对两种蓝藻(铜绿微囊藻和钝顶螺旋藻)和一种绿藻(斜生栅藻)的荧光光谱扫描,探索荧光分光光度法检测藻蓝蛋白含量的方法;完成对两种蓝藻(铜绿微囊藻和钝顶螺旋藻)和一种绿藻(斜生栅藻)的可见光吸光度光谱扫描,探索可见光分光光度法检测叶绿素a含量的方法。第二阶段建立蓝藻的荧光检测关系。培养两种蓝藻(铜绿微囊藻和钝顶螺旋藻)和一种绿藻(斜生栅藻)至生长稳定期,测量藻细胞浓度或长度、藻蓝蛋白荧光强度、叶绿素a可见光吸光度三个生物指标,建立藻蓝蛋白荧光强度、叶绿素a可见光吸光度分别对藻细胞浓度或长度的工作曲线。第三阶段研究不同生长条件的荧光检测关系。于不同光照强度下培养两种蓝藻(铜绿微囊藻和钝顶螺旋藻)至其生长稳定期,测定其藻细胞浓度或长度、藻蓝蛋白荧光强度、叶绿素a可见光吸光度三个生物指标,做出不同光照强度下两种蓝藻的藻蓝蛋白荧光强度工作曲线簇和叶绿素a可见光吸光度工作曲线簇,研究在不同光强下有着不同生长速率的蓝藻的光学特性的变化。第四阶段研究不同生长阶段的荧光检测关系。培养两种蓝藻(铜绿微囊藻和钝顶螺旋藻)一个生命周期,做出其生长曲线,选取其生命周期中的不同生长阶段的藻液,测定其藻细胞浓度或长度、藻蓝蛋白荧光强度、叶绿素a可见光吸光度三个生物指标,做出不同生长阶段中两种蓝藻的藻蓝蛋白荧光强度工作曲线簇和叶绿素a可见光吸光度工作曲线簇,研究不同生长阶段中有着不同生长速率的蓝藻的光学特性的变化。
本课题所得结论如下:
(1)建立蓝藻的荧光检测方法:通过荧光光谱扫描,探索得到荧光分光光度法检测藻蓝蛋白的方法,藻蓝蛋白的最佳荧光激发波长为630nm,最佳荧光发射波长为650nm,通过可见光光谱扫描,探索得到可见光分光光度法检测叶绿素a的方法,叶绿素a的最佳可见光吸收波长为682nm。
(2)建立蓝藻的荧光检测关系:做出铜绿微囊藻工作曲线,探索得到藻细胞浓度在105cell/mL-107cell/mL范围内,藻蓝蛋白荧光强度、叶绿素a可见光吸光度均与藻细胞浓度呈线性增长的关系;做出钝顶螺旋藻工作曲线,探索得到藻细胞长度在102mm/mL-105mm/mL范围内,藻蓝蛋白荧光强度、叶绿素a可见光吸光度均与藻细胞长度呈线性增长的关系;做出斜生栅藻工作曲线,探索得到藻细胞浓度在105cell/mL-107cell/mL范围内,叶绿素a可见光吸光度与藻细胞浓度呈线性增长关系,但是由于绿藻不含有藻蓝蛋白,所以藻蓝蛋白荧光强度值很小,趋于不变,可以忽略不计。
(3)研究不同生长条件的荧光检测关系:做出不同光照强度下两种蓝藻的藻蓝蛋白荧光强度工作曲线簇和叶绿素a可见光吸光度工作曲线簇。实验表明,随着光照强度的逐渐增大,两种蓝藻的工作曲线逐级下降,曲线斜率逐渐减小,即单位藻细胞中的藻蓝蛋白含量逐渐减少,叶绿素a含量也逐渐减少。
(4)研究不同生长阶段的荧光检测关系:培养两种蓝藻一个生命周期,连续监测两种蓝藻的藻细胞浓度或长度,做出两种蓝藻的生长曲线,将其生命周期分为四个阶段——迟缓期、生长期、稳定期和衰亡期。做出不同生长阶段中两种蓝藻的藻蓝蛋白荧光强度工作曲线簇和叶绿素a可见光吸光度工作曲线簇。实验表明,从迟缓期到生长期再到稳定期,工作曲线先抬升后下降,曲线斜率先增大后减小,即单位藻细胞中藻蓝蛋白含量从迟缓期到生长期逐渐上升,从生长期到稳定期逐渐下降,叶绿素a含量的变化趋势也相同。同时预测衰亡期,单位藻细胞中的藻蓝蛋白含量和叶绿素a含量将降低。
7.2展望
本实验所研究的是应用荧光分析技术检测蓝藻生物量。荧光分析技术的设备简单、操作方便、准确性高、价格低廉,可以实现藻类的实时、连续的原位监测。本实验已取得的研究结论表明,在实验室条件下荧光分析技术对纯培养的单种蓝藻的检测准确有效。然而在现实条件下,江河湖海的水质情况复杂而多变,一方面藻类种类繁多,即便是以蓝藻为主的江河湖海,也有多种不同蓝藻同时存在,另一方面藻类的生理特性随着季节气候的变化而变化,随着地理位置的不同而不同,如何在现实条件下根据不同的实际情况,修正荧光分析技术检测蓝藻的工作曲线,使其能够切实可行的运用于现实中,是下一步研究的主要内容。
下一篇:荧光检测藻蓝蛋白—译文及原文3
实验仪器
站内导航
如何付款
如何来访
运输及费用
友情链接
ENGLISH
集团网站
无锡建仪实验器材有限公司 地址:无锡市滨湖区蠡湖商务园35号 邮编:214125
电话:0510-85191518 传真:0510-85191517 邮箱:wx_jy17@163.com
版权所有,未经允许不得使用本站商标图片和文章
苏ICP备13061772号-3
 苏公网安备 32021102001268号
苏公网安备 32021102001268号
